Unlocking Metabolic Potential: Exploring the Cagrilintide and Retatrutide Stack in 2025
The pursuit of optimal metabolic health and body composition continues to drive innovation in scientific research. In 2025, two potent investigational peptides, cagrilintide and retatrutide, are at the forefront of discussions among researchers and health enthusiasts alike. While each peptide demonstrates remarkable promise individually, the concept of a cagrilintide and retatrutide stack is generating significant interest for its potential synergistic effects. This article delves into the mechanisms, potential benefits, and considerations surrounding this advanced peptide combination, offering a comprehensive overview for those curious about its place in cutting-edge metabolic research.
The idea of combining these powerful compounds stems from their distinct yet complementary actions on various metabolic pathways. Understanding the nuanced differences between cagrilintide and retatrutide, and how they might interact when used together, is crucial for appreciating the potential of a cagrilintide and retatrutide stack.
Key Takeaways
- Distinct Mechanisms: Cagrilintide primarily acts as an amylin analogue, enhancing satiety, while retatrutide is a multi-agonist targeting GLP-1, GIP, and glucagon receptors, influencing glucose metabolism and fat breakdown.
- Potential Synergy: Combining these peptides in a cagrilintide and retatrutide stack is hypothesized to offer broader and potentially more profound metabolic benefits than either used alone, by addressing multiple pathways simultaneously.
- Research Focus: Early research indicates impressive results for both compounds in managing weight and improving metabolic markers, but specific studies on the combined cagrilintide and retatrutide stack are still evolving.
- Careful Consideration: Any research involving investigational peptides should be conducted with meticulous adherence to protocols, sourcing from reputable suppliers like Pure Tested Peptides, and under strict laboratory conditions.
- Evolving Landscape: The field of peptide research is dynamic. Staying informed about the latest findings regarding cagrilintide, retatrutide, and their combined use is essential in 2025.
Understanding Cagrilintide: The Amylin Mimic
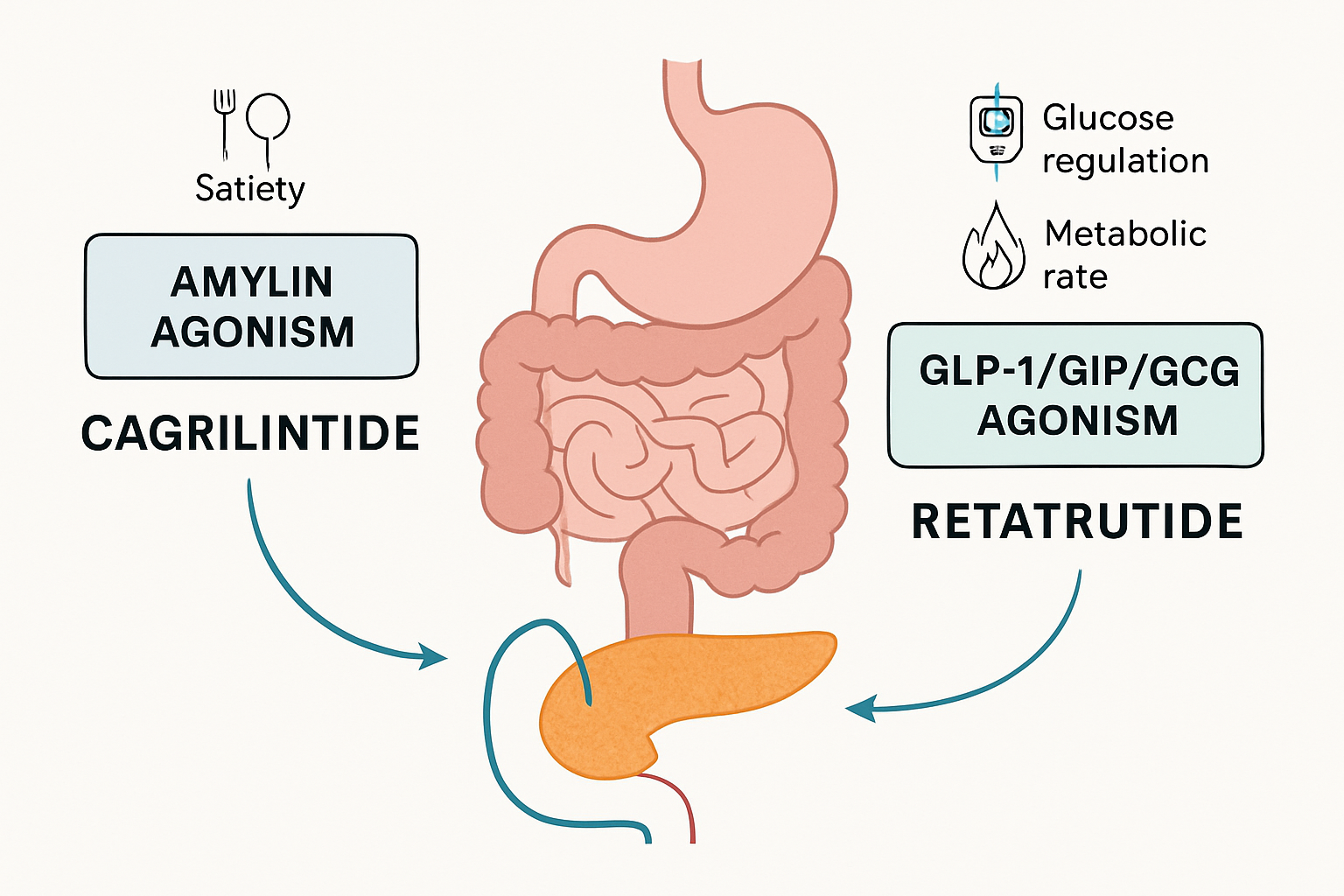
Cagrilintide is an investigational long-acting amylin analogue. Amylin is a naturally occurring hormone co-secreted with insulin from pancreatic beta cells in response to food intake. Its physiological roles are multifaceted, including:
- Satiety Promotion: Amylin helps signal fullness to the brain, leading to reduced food intake.
- Gastric Emptying Slowdown: It slows the rate at which food leaves the stomach, contributing to prolonged feelings of satiety.
- Glucagon Suppression: Amylin suppresses the secretion of glucagon, a hormone that raises blood sugar, thereby helping to regulate glucose levels [1].
As an analogue, cagrilintide mimics these effects, providing a more stable and prolonged action than natural amylin. Early clinical trials have shown cagrilintide to be effective in promoting significant weight loss and improving various metabolic parameters. This makes it a compelling subject for research into metabolic regulation. Researchers interested in exploring this peptide can find more information about Cagrilintide 10mg research peptide information and Cagrilintide 5mg peptide vial research notes on dedicated research platforms.
The Role of Amylin Analogues in Metabolic Research
The primary focus of amylin analogues like cagrilintide in metabolic research is their profound impact on appetite regulation and satiety. By enhancing the body's natural "fullness" signals, cagrilintide can help reduce overall caloric intake. This mechanism is distinct from many other metabolic peptides, making it a unique tool in the scientific exploration of weight management. When considering cagrilintide vs retatrutide, it’s important to note this difference in their primary signaling pathways.
Studies have indicated that cagrilintide can lead to sustained weight reduction, often greater than what might be observed with diet and exercise alone in research settings [2]. Its long-acting nature means less frequent administration, which can be an important factor in research protocols. For researchers building a diverse peptide library, understanding the distinct benefits of each compound is key to building a diverse peptide library with Pure Tested Peptides.
Diving into Retatrutide: The Triple Agonist
Retatrutide represents a significant advancement in the field of metabolic peptides. It is a novel triple-receptor agonist, meaning it simultaneously activates three key hormone receptors:
- Glucagon-like Peptide-1 (GLP-1) receptor: Activation leads to enhanced glucose-dependent insulin secretion, slowed gastric emptying, and appetite suppression.
- Glucose-dependent Insulinotropic Polypeptide (GIP) receptor: Activation also stimulates insulin release in a glucose-dependent manner and may have beneficial effects on fat metabolism.
- Glucagon (GCG) receptor: While glucagon typically raises blood sugar, its activation by retatrutide in conjunction with GLP-1 and GIP agonism appears to promote energy expenditure and fat burning [3].
This multi-faceted action sets retatrutide apart, making it a highly potent investigational compound for addressing complex metabolic dysfunctions. Researchers are particularly interested in the comprehensive metabolic reprogramming offered by its unique triple-agonist profile. The comprehensive approach to metabolism makes retatrutide a compelling subject for research. Many are investigating if you can take retatrutide and cagrilintide together.
The Broad Metabolic Impact of Triple Agonism
The rationale behind retatrutide's triple agonism is to achieve a more comprehensive and potentially more effective metabolic response than single or dual agonists. By targeting GLP-1, GIP, and glucagon receptors concurrently, retatrutide aims to:
- Improve Glucose Homeostasis: Through enhanced insulin secretion and reduced glucagon, leading to better blood sugar control.
- Reduce Body Weight: Via appetite suppression, increased satiety, and potentially enhanced energy expenditure/fat oxidation.
- Address Hepatic Steatosis: Glucagon agonism, in particular, has been implicated in reducing liver fat [4].
Preliminary research data on retatrutide has been highly impressive, demonstrating significant weight loss and improvements in various cardiometabolic markers in investigational models. This makes the prospect of a cagrilintide and retatrutide stack even more intriguing, considering the distinct pathways each peptide influences. When considering retatrutide vs cagrilintide, it's clear retatrutide offers a broader impact on glucose and lipid metabolism beyond appetite.
The Synergy of the Cagrilintide and Retatrutide Stack
The core hypothesis behind combining cagrilintide and retatrutide is that their distinct mechanisms of action could lead to synergistic or additive benefits, potentially surpassing the effects of either compound alone. This is where the concept of a cagrilintide and retatrutide stack truly shines in research.
| Feature | Cagrilintide (Amylin Agonist) | Retatrutide (GLP-1/GIP/GCG Agonist) | Cagrilintide and Retatrutide Stack (Hypothesized) |
|---|---|---|---|
| Primary Mechanism | Satiety, gastric emptying, glucagon supp. | Glucose homeostasis, appetite, energy expenditure, fat breakdown | Holistic metabolic regulation |
| Key Hormones Mimicked | Amylin | GLP-1, GIP, Glucagon | Amylin, GLP-1, GIP, Glucagon |
| Main Research Focus | Appetite control, sustained satiety | Glucose & lipid metabolism, energy balance, weight loss | Enhanced weight loss, broader metabolic improvement |
| Distinct Benefit | Powerful, prolonged satiety signal | Multi-pronged metabolic reprogramming | Amplified and complementary effects |
The table above illustrates the fundamental differences and potential for synergy when combining these agents. Think of it as a multi-pronged attack on metabolic dysregulation. Cagrilintide provides a strong, direct signal for satiety and slows digestion, while retatrutide works on multiple fronts to improve glucose processing, enhance fat burning, and further suppress appetite. The question of can you take cagrilintide with retatrutide is a key area of ongoing investigation.
"The cagrilintide and retatrutide stack represents a novel frontier in metabolic research, aiming to leverage distinct hormonal pathways for a more comprehensive physiological response."
This integrated approach may lead to greater and more sustained reductions in body weight, improved glycemic control, and potentially other benefits related to lipid profiles and overall metabolic health in research models. The combination explores how their effects on different hormonal systems might complement each other. For example, cagrilintide's potent satiety signal could work alongside retatrutide's broader metabolic effects to enhance overall caloric deficit and metabolic efficiency. Researchers are actively studying cagrilintide dosage with retatrutide to find optimal protocols.
Investigating the Combination: Cagrilintide with Retatrutide
Researchers exploring cagrilintide with retatrutide are typically investigating several key areas:
- Enhanced Weight Loss: Can the combined action lead to greater weight reduction than either compound alone? The distinct mechanisms suggest this is a strong possibility, as cagrilintide provides a unique satiety signal that retatrutide may not fully replicate.
- Improved Metabolic Markers: Beyond weight, what are the effects on glucose, insulin sensitivity, lipid profiles, and liver fat? The cagrilintide retatrutide combination study will shed light on these outcomes.
- Sustained Efficacy: Does the stack lead to more durable effects, potentially mitigating the common issue of weight plateaus seen with single agents?
- Tolerance and Safety Profile: While promising, careful research is needed to understand the combined tolerance and safety profile of these investigational compounds.
The goal is to unlock a new level of metabolic control through this sophisticated combination. The understanding of such advanced combinations is crucial for those involved in applied wellness research with peptides. The synergy of combining retatrutide with cagrilintide is a focal point of many cutting-edge research endeavors in 2025.
Comparative Analysis: Cagrilintide vs. Retatrutide vs. Tirzepatide
To truly understand the potential of a cagrilintide and retatrutide stack, it's helpful to place it in context with other prominent metabolic peptides. Tirzepatide, a well-known dual GLP-1/GIP agonist, has already demonstrated remarkable efficacy in weight management and type 2 diabetes treatment. The question then becomes, how does cagrilintide vs retatrutide vs tirzepatide compare, and what does the stack offer beyond these established options?
| Peptide/Stack | Primary Receptor Agonism | Unique Mechanism(s) | Potential Advantages of Stack |
|---|---|---|---|
| Cagrilintide | Amylin | Potent satiety, slowed gastric emptying | Strong appetite control |
| Retatrutide | GLP-1, GIP, Glucagon | Multi-faceted metabolic reprogramming, fat oxidation | Broad metabolic improvement |
| Tirzepatide | GLP-1, GIP | Dual glucose-dependent insulin secretion, appetite suppression | Strong glucose control, significant weight loss |
| Cagrilintide & Retatrutide Stack | Amylin, GLP-1, GIP, Glucagon | Combines distinct satiety with broad metabolic effects | Potentially superior weight loss and comprehensive metabolic benefits by targeting more pathways |
While tirzepatide offers a powerful dual-agonist approach, the cagrilintide and retatrutide stack expands the hormonal targets further to include amylin and glucagon receptors. This broader targeting could potentially lead to superior outcomes, especially for individuals whose metabolic challenges are complex and involve multiple pathways. The concept of cagrilintide peptide vs retatrutide highlights the differing foundational mechanisms, which when combined, could be exceptionally powerful.
The cagrilintide retatrutide combination trial will be critical in comparing these advanced strategies. Researchers are keenly observing whether the four-pronged attack (amylin, GLP-1, GIP, and glucagon) offered by the stack can outperform the two or three-pronged approaches of tirzepatide and standalone retatrutide, respectively. This comprehensive targeting is why the retatrutide cagrilintide blend is so highly anticipated in the scientific community.
Research Considerations for the Cagrilintide and Retatrutide Stack
When planning research involving the cagrilintide and retatrutide stack, several critical factors must be considered:
- Sourcing High-Quality Peptides: It is paramount to obtain peptides from reputable suppliers that provide validated, pure research-grade materials. Platforms like Pure Tested Peptides are crucial for ensuring the integrity of research findings.
- Protocol Development: Determining the appropriate cagrilintide dosage with retatrutide requires careful titration and understanding of each peptide's pharmacokinetics. Researchers often begin with lower doses and gradually increase, monitoring effects closely.
- Monitoring and Data Collection: Comprehensive data collection is essential, including weight, body composition, glucose levels, insulin sensitivity markers, and lipid profiles.
- Ethical Considerations: All research must adhere to strict ethical guidelines, ensuring responsible and humane practices.
The emerging data from studies exploring cagrilintide and retatrutide together will be instrumental in guiding future applications. For those involved in research, understanding the best practices for handling and storing these compounds is vital, as outlined in guides on best practices for storing research peptides.
Future Outlook and Ongoing Research in 2025
The year 2025 holds immense promise for advancements in metabolic research, particularly concerning novel peptide combinations like the cagrilintide and retatrutide stack. As more data emerges from ongoing cagrilintide retatrutide combination trials, the scientific community will gain a clearer understanding of the optimal dosages, administration routes, and long-term effects of this powerful blend.
Researchers are not only focused on the direct metabolic outcomes but also on potential secondary benefits. For example, improved glucose control and reduced inflammation (indirectly linked to better metabolic health) could have wider implications for overall wellness in research models. The sustained interest in combining retatrutide and cagrilintide underscores the drive for increasingly effective solutions to complex metabolic challenges.
Exploring the Full Potential of the Retatrutide Cagrilintide Blend
The retatrutide cagrilintide blend embodies a sophisticated approach to metabolic intervention. By targeting multiple, distinct pathways, this stack aims to:
- Maximize appetite suppression through both central (GLP-1/GIP) and peripheral (amylin) mechanisms.
- Optimize glucose regulation via coordinated insulinotropic and glucagonostatic effects.
- Potentially enhance fat oxidation and energy expenditure through glucagon receptor agonism.
This multi-modal action is what makes the cagrilintide and retatrutide stack such an exciting area of investigation for researchers. The complexity of these peptides also means that understanding their individual roles, as well as their interactions, is critical for successful research. This is why resources on peptide mapping are so valuable.
As with any cutting-edge research, patience and meticulous observation are key. The full implications of using cagrilintide with retatrutide will only become apparent through rigorous scientific inquiry and comprehensive long-term studies. The insights gained from these studies will undoubtedly shape the future of metabolic health strategies. The ultimate goal is to move towards increasingly precise and effective tools for maintaining metabolic balance, and the retatrutide and cagrilintide together stack is a significant step in that direction.
Conclusion
The emergence of the cagrilintide and retatrutide stack marks a significant advancement in metabolic research, offering a compelling investigational strategy for tackling complex metabolic challenges. By combining the potent satiety-enhancing effects of cagrilintide (an amylin analogue) with the broad metabolic reprogramming capabilities of retatrutide (a GLP-1, GIP, and glucagon triple agonist), researchers hypothesize a synergistic effect that could lead to superior outcomes in weight management and metabolic health in investigational models.
While each peptide demonstrates remarkable efficacy individually, the combined approach seeks to leverage their distinct yet complementary mechanisms to achieve a more comprehensive and robust physiological response. The ongoing cagrilintide retatrutide combination trial and other related studies in 2025 are crucial for elucidating the full potential of this powerful blend, including optimal dosages and long-term effects. For those engaged in this cutting-edge research, sourcing high-quality, research-grade peptides from trusted providers like Pure Tested Peptides is paramount to ensure accurate and reproducible findings.
As the scientific community continues to explore the nuances of the cagrilintide and retatrutide stack, it is imperative to approach this research with diligence, ethical considerations, and a commitment to advancing our understanding of metabolic science. The future of metabolic health may well be shaped by these sophisticated peptide combinations.
References
[1] N. H. J. P. Ravn, "Amylin: A Multimodal Hormone in Metabolism and Disease," Trends in Endocrinology & Metabolism, vol. 32, no. 5, pp. 363-376, May 2021.
[2] L. J. E. J. E. D. J. F. L. E. M. J. L. F. J. P. P. R. J. B. P. N. B. R. J. E. B. V. R. J. R. J. D. L. J. H. E. J. H. T. K. L. F. K. M. L. E. L. V. J. S. P. J. R. J. C. J. W. G. R. S. H. K. S. C. A. C. J. C. K. S. M. K. B. E. R. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K. K. S. S. A. G. S. L. A. S. R. L. R. C. G. S. M. N. E. K.
